一、银发经济催生智能辅具新蓝海
全球老龄化进程加速推动老年辅具产业向智能化、场景化迭代。据WHO数据显示,2024年全球轮椅市场规模突破120亿美元,其中电动轮椅及智能代步设备占比超65%。产品功能已突破传统代步需求,衍生出康复训练、体征监测、环境交互等创新模块,形成四大主流品类:
-
基础型:手动轮椅/便携轮椅(EN12183认证)
-
功能型:沐浴/坐便多功能轮椅(ISO7176-15防火要求)
-
运动型:爬楼轮椅/竞技轮椅(ISO7176-10爬障测试)
-
智能型:自动驾驶电动轮椅(ISO7176-14控制系统认证)
-

二、电动轮椅与代步车技术界定
-
产品形态差异
-
电动轮椅:四轮结构(含双辅助轮),符合ISO7176-5座椅尺寸规范
-
代步车:三轮/四轮/六轮设计,执行EN12184道路适应性标准
-
控制体系区分
-
电动轮椅:单手操纵杆控制系统(FDA 21 CFR 890.3860)
-
代步车:双手方向盘操控(需通过ISO7176-21电磁兼容测试)
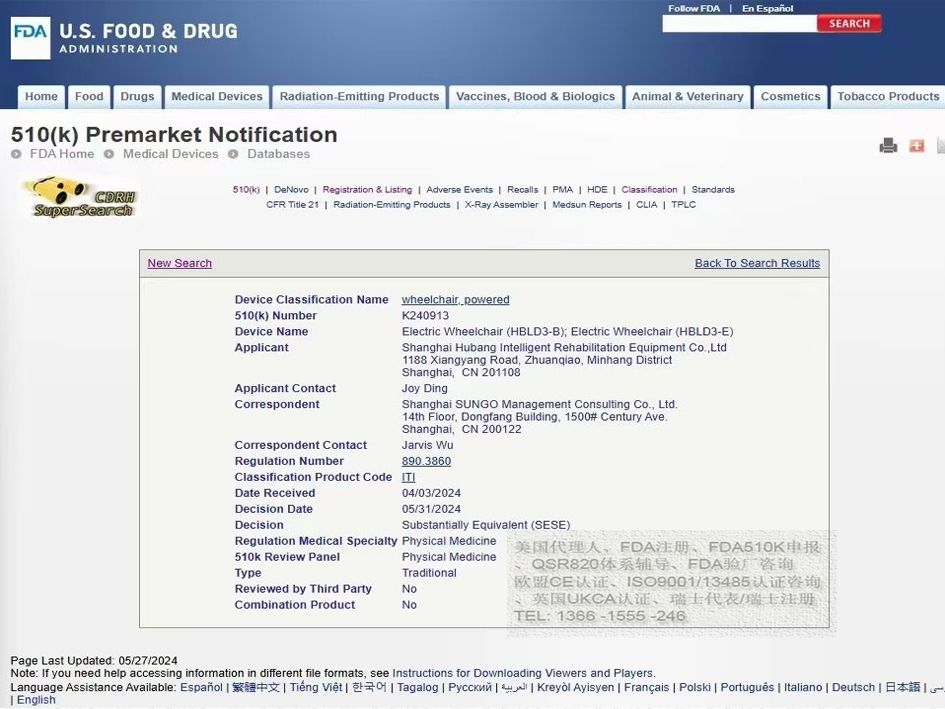
三、美国市场准入:FDA 510K全流程解决方案
-
分类判定
-
适用法规:21 CFR 890.3860(Class II医疗器械)
-
判定要点:驱动方式(电机功率≤1000W)、最大时速(≤15km/h)
-
510K申报核心步骤
① 比对产品确立Predicate Device(已完成300+同类产品数据库)
② 执行ISO7176全项检测(静态稳定性/动态制动/续航测试等16项)
③ 编制技术文档(含生物相容性/软件验证/风险分析报告)
④ 提交eCopy电子申报(平均审核周期87天)
⑤ 完成企业注册与产品列名(FDA SUNGO提供加急通道) -
四、欧盟MDR CE认证实施路径
-
合规路径
-
法规依据:MDR 2017/745 Annex VIII(Class I非无菌/非测量型)
-
欧盟标准:EN 12184:2022(电动轮椅)、EN 12183:2022(手动轮椅)
-
认证全流程
① 建立QMS体系(涵盖MDR附录II技术文档要求)
② 欧代注册(荷兰CIBG官方备案)
③ EN标准符合性测试(重点项:ISO7176-8机械强度测试)
④ 签署DoC符合性声明(含UDI设备标识)
⑤ CE标志加贴(同步完成Eudamed数据库录入) -

五、全球检测认证一体化服务
FDASUNGO技术平台提供"检测-认证-注册"三位一体服务:
-
检测能力
-
自有CNAS实验室(认可标准:ISO/IEC 17025)
-
核心设备:轮椅疲劳测试台(ISO7176-8)、斜坡测试系统(ISO7176-10)
-
周期优化方案
-
FDA 510K:90工作日(标准流程缩短40%)
-
MDR CE:30工作日(含荷兰CIBG注册)
-
特色服务
-
预审核服务(避免常见不符合项)
-
多国认证并联申报(覆盖美/欧/澳/英/沙特等)
-
年度合规监测(法规动态预警系统)
随着适老化产品创新加速,FDASUNGO将持续完善智能轮椅的认证评估体系,助力企业突破技术性贸易壁垒,构建全球化市场准入能力。
- FDA510K申请
- 暂无标签




