引言:
近期,欧盟各国家主管当局加大了对于市场上医疗器械的监管。各个国家当局的监管方式稍有不同,但是很多方式都类似:发现市场上有产品的标签不符合法规要求,责难欧盟代表->联想是不是制造商不知道法规要求->是不是产品本身质量也不符合欧洲要求->做产品测试。另外,也发生过由于标签不符合法规要求而导致货物卡在欧洲海关不被放行的情况。建议医疗器械的法定制造商,在产品出口欧洲时候,一定要非常重视,标签应该符合适用的法规要求,谨防发生上述事件。
在此准备了一个中盒的例子,向您简单介绍一下欧洲对于标签的法规要求。请注意口罩只是举例,下面的解释适用于所有产品,不限于口罩。
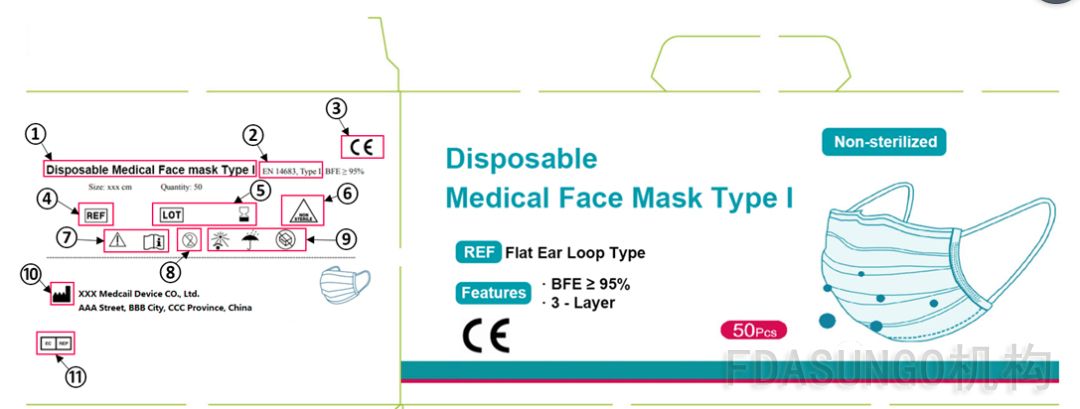
① 产品名称,(以及所有其他的信息,比如产品描述,预期用途,warning等等)必须有销售目的地国家的语言。这是MDD/MDR附录I的要求。
② 这是产品标准的特别要求。医用口罩的欧洲标准EN 14683中,要求把EN 14683,以及口罩的类型(Type I, 或者Type II,或者Type IIR)打印在标签上。如果加上标准的版本号也是可以的,全部应为EN 14683:2019+AC:2019。
③ CE标识,这是MDD 附录XII,以及MDR附录V的要求。请注意这个CE标识的比例和形状都不可以改变,只可以等比例的缩放,而且不可以矮于5毫米。请看附件MDD法规的最后一页。
④ 这个标识的意思是产品的“品号”,如果产品的名称或者型号可以完全识别产品, 那么品号就不是必须的。
⑤ 这些标识是产品的“批号”和“有效期”。这是MDD/MDR附录I的要求。
⑥ 这是“非灭菌产品”的标识。请注意如果是灭菌的口罩,那么需要公告机构出具CE证书,才可以销售,而普通的一类产品(比如非灭菌口罩)不需要CE证书。
⑦ 这两个,分别是“警告”和“查看使用说明书”的标识。如果此产品有说明书,以及说明书中有“警告”信息的,那么在标签上需要打印这些标识。当然,如果此产品没有说明书或者没有警告信息,那么就不需要这些标识了。
⑧ 这是“禁止二次使用”的标识。
⑨ 这里是一些例子,关于存储环境和条件的要求。请注意,这些不是欧洲法规的明确要求,而是制造商自己基于风险分析,产品检测等等,做出的决定。MDD/MDR附录I的要求仅仅是,如果对于产品防护,从技术上有相应的存储环境/存储条件等要求,那么这些要求应该体现在包装上,提示给用户。
⑩ 这个标识是“法定制造商”的意思。请注意这里必须写法规定义里的“法定制造商”,也就是声称对于此产品负责,并且跟我司签订了欧盟代表协议,进行了产品注册的公司。这里所指的不是生产产品的公司,也不是销售代理公司。这是MDD/MDR附录I的要求。
⑪ 这个是“欧盟代表”的名称和地址。当产品有CE标识的时候,欧盟代表的信息,必须同时出现的标签上。不可以产品有CE标识,但是欧盟代表信息不在包装上。这是MDD/MDR附录I的要求。
以TYPE I 的医用口罩为例,以上①②③⑤⑥⑧⑩⑪涉及的信息,必须出现在包装的中盒上。④⑦⑨的信息如果适用,也应当出现在此包装上。这些标识,都可以在ISO15223标准当中找到(由于版权问题,请您自行查找,获取该标准)。我司推荐尽量使用这些标识。因为如果使用语言描述,那么按照法规要求,这些语言都要翻译成目的地国家的语言。
- ISO13485
- 暂无标签
