
IVDR将于2022年5月26日强制执行,很多体外诊断试剂厂商觉得时间还早,FDASUNGO却深深觉得已经不早了,因为相比较MDR对于医疗器械企业的影响,IVDR对于体外诊断试剂的厂商影响更大。为什么呢? IVDD时代只有20%左右的体外诊断试剂是需要公告机构发证的,还有80%企业可以自我声明。到了IVDR这两个比...

早在数周前,FDASUNGO荷兰公司已经为国内器械厂商成功申请IVDR CE注册证书。同时,SUNGO德国也已经受理部分厂商的IVDR CE注册申请。除了提供欧盟授权代表和注册服务,我们还提供IVDR技术文件编撰服务,帮助制造商全面规避合规风险。1 哪些IVD属于Class A类呢?IVDR法规共有7条分类规则 IVD...
为了避免和病人直接接触,医生在为病人检查时需要带手套,该手套可以是检查手套或外科手套,材质通常为乳胶,丁腈或者PVC材料,有一定的拉伸性能,有灭菌的不灭菌的。该检查手套虽然属于FDAI类产品,但是仍需要提交510k上市前评估。下面我们就来看下丁腈手套美国的fda510k申请流程。 丁腈手套FDA510k生物相容性...

ISO13485标准是适用于医疗器械法规环境下的质量管理体系标准,其全称是《医疗器械质量管理体系 用于法规的要求》。 它采用了基于ISO9001标准中PDCA的相关理念,相较ISO9001标准适用于所有类型的组织,ISO13485更具有专业性,重点针对与医疗器械设计开发、生产、贮存和流通、安装、服务和停用及处置等相...

出口欧盟的CE(MDR)注册流程厂家开始投入欧盟市场,产品进入欧盟需要做CE认证,满足欧盟医疗器械法规(MDR)要求。下面以医用口罩为例出口欧盟MDR CE认证的申请流程。医用手术胶带绷带创可贴口罩等产品出口欧盟,按照医疗器械法规MDR分为两类,无菌类和非灭菌两大类。1、如无菌类口罩的话:分类1S,需要公告机构介入。2...

医用口罩在FDA属于非510(K)豁免的产品,不仅需要进行工厂注册和产品列名,还要编写FDA510(K)文件,提交FDA 审核,审核通过后才可进入美国市场。1)公司配合提供产品材料,由我司进行分类和确认;2)我司提供编制FDA510K技术文件所需的根本产品信息和文件。贵公司依据清单准备检测资料和相关产品;3) FDA5...

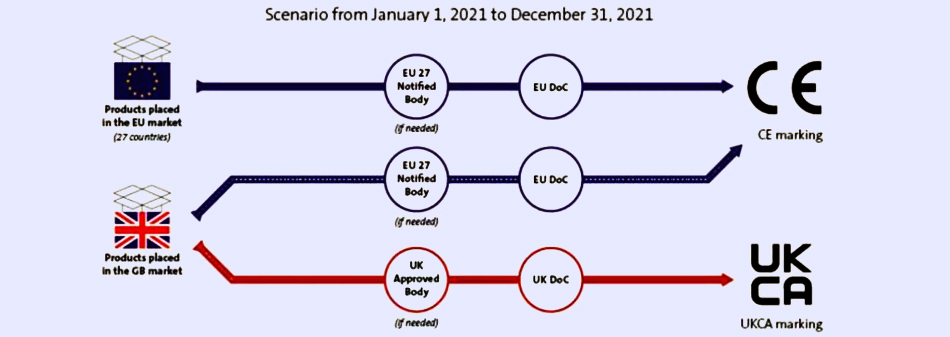
2021年1月1日起,UKCA标志将正式使用众所周知,英国已经脱欧,目前正处于脱欧过渡期中,该过渡期将到2020年年底为止。根据英国政府9月1日的公告可知,自2021年1月1日开始UKCA标志将正式开启使用。大多数目前在CE标志管控范围内的产品将来如果要出口到英国市场(英格兰,威尔士以及苏格兰),都必须加贴UKCA标志...

2017年5月5日,欧盟正式发布了新版医疗器械法规MDR(EU 2017/745),法规过渡期为3年,2020年5月26日开始强制执行,不过2020年4月24日,欧盟宣布将《医疗器械法规(MDR)》强制实施日期推迟一年,于2021年5月26日正式实施。 据悉,《医疗器械法规(MDR)》是一份550多页的...

实验室耗材出口欧洲,要做CE ISO证书,要怎么操作?CE产品是实验室耗材:载玻片、盖玻片、试管、离心管、吸头、量杯、培养皿、包埋盒、吸管、拭子、试管塞、存储盒、试管架、采样棒、药棉、量筒、烧杯、漏斗、真空采血管等产品,欧盟属于CLASS I。MDR法规下的DOC和MDD指令的DOC不是一样的概念从法规来说,I类普通器...
MHRA 机构介绍 MHRA 的全称是Medicinesand Healthcare products Regulatory Agency医药和健康产品管理局。MHRA是属于英国的主管药品和医疗器械的政府部门。在英国脱欧后,医疗器械的上市前和上市后的监管都将由MHRA主管,其性质类似于美国FDA或者国内的NMPA。...
2020年是个鼠年,不一样的鼠年。凶猛的疫情,让我们过了一个不一样的年。我们天天在家呆,在家玩,无聊的很。现在疫情控制住了,防疫产品出口欧盟CE认证MDD/MDR,PEE口罩、护目镜、防护衣,额温枪的产品可以做计划出口了。2020年医用防疫产品出口欧盟口罩、手套、核酸检测试剂盒等产品的要求越来越难,程序现在很严格,没...

欧盟CE认证是一种安全认证标志,被视为制造商打开并进入欧洲市场的护照。在欧盟市场流通的产品,不论是欧盟内部企业生产还是其他国生产,必须加贴“CE”标志,以表明产品符合欧盟《技术协调与标准化新方法》指令的基本要求。体外诊断CE认证:一、关于体外诊断医疗器械 (IVDD 98/79/EC)指令:98/79/EC体外诊断医疗...

FDASUNGO机构隶属于上海沙格医疗科技有限公司,创建于2006年,立志于成为全球化的医疗器械法规技术服务商。 目前FDASUNGO机构在中国、欧洲、北美、沙特和澳洲均设有服务机构,服务过的客户更是覆盖了亚洲(中国、越南、马来西亚、孟加拉、新加坡)、欧洲(英国、瑞士、瑞典、丹麦、挪威)、北美(美国、加拿大)、南美(阿...
防护口罩、防护手套归属于PPE个人防护指令管控范围,而医用口罩、医用手套则归属于MDD指令/ MDR法规医疗器械质量的管控范围,所以不管是防护还是医用,出口欧盟都是必须要做CE认证。 医用检查手套、PVC手套,丁睛手套丁腈橡胶是由丁二烯和丙烯腈经乳液聚合法制得的,其制品耐油性极好,耐磨性较高,耐热性较好。采用优质的...

丁腈橡胶 是由丁二烯和丙烯腈经乳液聚合法制得的,其制品耐油性极好,耐磨性较高,耐热性较好。采用优质的丁腈橡胶配以其他的助剂,精制加工而成;不含蛋白质,对人体皮肤无过丁腈橡胶是由丁二烯和丙烯腈经乳液聚合法制得的,其制品耐油性极好,耐磨性较高,耐热性较好。采用优质的丁腈橡胶配以其他的助剂,精制加工而成;不含蛋白质,对人体皮...