前言:
近期,全球新冠疫情迅速蔓延。欧洲美国作为重灾区,对于新冠病毒检测试剂的需求及其旺盛,国内制造商出口欧盟的意向日益增强。故,业内对新冠病毒检测试剂类产品CE认证关注度越来越高。
新冠病毒检测试剂需要符合的欧盟指令是IVDD(98/79/EEC)体外诊断器械指令,按照IVDD指令中的分类要求,新冠病毒检测试剂的分类是Others类(其他类)。
根据分类,欧盟IVDD 指令中非Others 类产品,如List A,List B,Self-testing,需要由第三方NB 机构(如:TUV,Dekra,BSI)执行审核发证流程,通过欧颁发带有NB 号的CE 证书。按照现行的欧盟医疗器械法规,此路径获取CE 证书的时间至少10~15 个月以上,总费用超300,000 RMB。
根据分类,欧盟IVDD 指令中属于Others 类产品,按照指令要求,公告机构不可强制介入Others 类器械的发证事宜,制造商基于完整的CE 技术文档宣称符合CE(自我CE 符合性声明格式如下)。也即,制造商无法要找发证机构去申请带NB 号的CE 证书,制造商根据自己出具自我CE 符合性声即可打上CE mark,出口欧盟。在欧盟有经销活动前,需要委托欧盟授权代表去当地主管机构做登记,整个欧盟28 个成员国,只需登记一次。
简而言之,对于Others类IVDD产品,制造商满足:CE技术文档+CE自我符合性声明+欧盟代表注册即已符合CE(前提是制造商按照ISO 13485要求规范生产),无公告机构发证,也没有带NB号的CE证书。
截至目前,国内多家体外诊断(IVD)企业宣布其新冠病毒检测产品获得欧盟准入资格或CE证书,进入国际新冠病毒体外诊断市场!企业包括华大基因、上海之江、青岛汉唐、万孚生物、美康生物、圣湘生物、迈克生物、亚辉龙、深圳新产业、达安基因、凯普生物、华迈兴微、一瑞生物、丹大生物、卓诚惠生、泰熙生物等。都是CE技术文档+CE自我符合性声明+欧盟代表注册这个合规路径。
I. 新冠病毒检测试剂产品CE符合性流程:
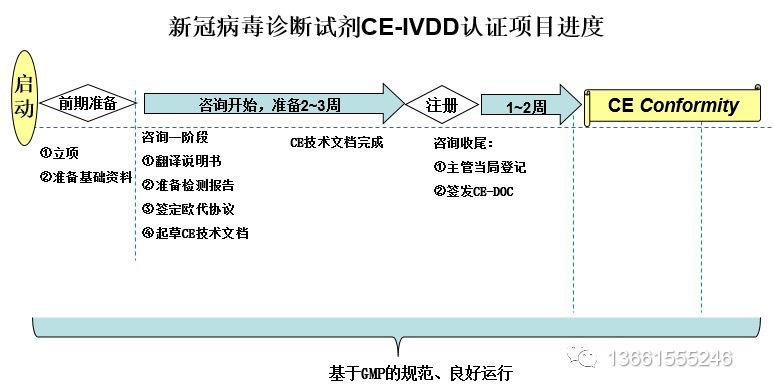
II.新冠病毒检测试剂企业申请CE需要提供的资料清单:
根据EN 13612:2002标准,试验举例:交叉试验,干扰试验,分析灵敏度,分析特异性试验,包括连续三批产品的检验记录,企业参考品的建立。
稳定性研究:根据标准EN 13640:2002,包含加速稳定性、实时稳定性、开瓶稳定性、模拟运输试验,等
文件
备注
说明书
根据EN ISO18113及EN ISO 15223等标准
标签
英文的(产品名称,规格型号,批号,效期,生产日期,生产信息(企业名称,地址,联系方式等信息),欧代信息,CE标识,外包装包含基本的标识)
技术要求
只需要技术指标及检验方法
性能评估
临床评价
不需要临床试验,类似于国内的免临床试验(需要方案及报告)
风险报告
根据EN ISO 14971:2012,特别是Annex H。
人源性组织或物质的说明
关键原料的供应商,关于生物安全性的说明
生产工艺流程图
/
III.新冠病毒检测试剂需要符合的欧盟协调标准清单
Standard/Directive Reference
Title
98/79/EC(IVD)
Directive 98/79/EC of the European Parliament and of the council of 27
EN ISO 13485: 2016
Medical devices-Quality management systems – Requirement for regulatory purposes.
EN 13612:2002
Performance evaluation of in vitro diagnostic medical devices
EN 13641: 2002
Elimination or reduction of risk of infection related to in vitro diagnostic reagents
EN 13975: 2003
Sampling Procedures used for Acceptance testing of in vitro diagnostic medical devices - Statistical aspects
EN ISO 14971:2012
Medical Devices - Application of Risk management to medical devices
EN ISO 15223-1: 2016
Medical devices – Symbols to be used with medical device labels, labelling and information to be supplied – Part 1: General requirements
EN ISO18113-1:2011
In vitro diagnostic medical devices. Information supplied by the manufacturer (labelling). Terms, definitions and general requirements
EN ISO18113-2:2011
In vitro diagnostic medical devices. Information supplied by the manufacturer (labelling). In vitro diagnostic reagents for professional use
EN 13640:2002
Stability testing of in vitro diagnostic reagents
EN ISO 23640:2015
In vitro diagnostic medical devices. Evaluation of stability of in vitro diagnostic
IV.新冠病毒检测试剂CE技术文档目录列表(建议):
1. 00 TCF Master File
2. 01 European Representative Agreement
3. 02 Harmonized standards list
4. 03.1 Instruction For Use
5. 03.2 Label
6. 04 Design and Manufacturing Information
7. 05 ER Checklist
8. 06 Risk analysis report
9. 07 Performance Analysis Related Research Data
10. 08 Stability Evaluation Report
11. 09 Key raw materials Suppliers and Biosafety Description
12. 10 Clinical Evaluation Report
13. 11 Declaration of Conformity
FDASUNGO作为欧盟法规第一线的服务公司,提供新冠病毒检测试剂欧盟CE技术文档辅导及欧盟授权代表和欧盟注册服务,为企业产品出口欧盟保驾护航!
- CE认证
- 暂无标签
